Em Sinapse no ENEM (Termoquímica) #37
(ENEM 2010) No que tange à tecnologia de combustíveis alternativos, muitos especialistas em energia acreditam que os álcoois vão crescer em importância em um futuro próximo. Realmente, álcoois como metanol e etanol têm encontrado alguns nicho...

|
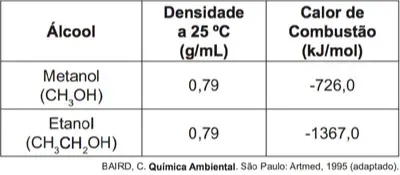
(ENEM 2010) No que tange à tecnologia de combustíveis alternativos, muitos especialistas em energia acreditam que os álcoois vão crescer em importância em um futuro próximo. Realmente, álcoois como metanol e etanol têm encontrado alguns nichos para uso doméstico como combustíveis há muitas décadas e, recentemente, vêm obtendo uma aceitação cada vez maior como aditivos ou mesmo como substitutos para a gasolina em veículos. Algumas das propriedades físicas desses combustíveis são mostradas no quadro seguinte.
|
Dados: Massas molares em g/mol: H = 1,0; C = 12,0; O = 16,0.
Considere que, em pequenos volumes, o custo de produção de ambos os álcoois seja o mesmo. Dessa forma, do ponto de vista econômico, é mais vantajoso utilizar
a) metanol, pois sua combustão completa fornece, aproximadamente, 22,7 kJ de energia por litro de combustível queimado.
b) etanol, pois sua combustão completa fornece, aproximadamente, 29,7 kJ de energia por litro de combustível queimado.
c) metanol, pois sua combustão completa fornece, aproximadamente, 17,9 MJ de energia por litro de combustível queimado.
d) etanol, pois sua combustão completa fornece, aproximadamente, 23,5 MJ de energia por litro de combustível queimado.
e) etanol, pois sua combustão completa fornece, aproximadamente, 33,7 MJ de energia por litro de combustível queimado.
Primeiro temos que calcular a energia liberada para cada litro de metanol e etanol queimado partir das densidades. A densidade do metanol e do etanol é 0,79 g/ml, então 1L desses combustíveis tem massa igual a 790 g.
Metanol:
1 mol de metanol tem massa igual a 32g. Logo, a quantidade de energia liberada pela queima de 1 litro de metanol é igual a:
32g.........................726 kJ
790g.........................X
X=17923 kJ ou 17,9 MJ
O mesmo será feito para o etanol.
Etanol:
1 mol de etanol tem massa igual a 46 g, então a quantidade de energia liberada na queima de 1 litro de etanol é igual a:
46g......................1367 kJ
790g...................Y
Y=23476 kJ ou 23,5 MJ
Como fizemos a comparação pros dois combustíveis como 1L o mais vantajoso é o etanol por liberar mais energia que metanol.
RESPOSTA: "D"
- Quer reconhecer ainda mais o nosso trabalho de divulgação e popularização da Ciência? Agora, com nossos posts aqui no Pingback, você pode nos doar R$ 1,00 por conteúdo ou mesmo se inscrever por R$ 5,00 ao mês ou R$ 50,00 ao ano.